近岸蛋白荣获CGCS 2025第六届国际细胞与基因治疗中国峰会暨展览会
“ CGT领域可靠原料与试剂供应启明星奖 ”

5月29-5月30日,CGCS 2025第六届国际细胞与基因治疗中国峰会暨展览会在南京扬子江国际会议中心隆重举办!此次CGCS 2025峰会云集200+全球发言嘉宾,100+主流展商,5000+行业专业人士线下参与,10000+全球观众线上参与,150+全球监管机构与产业领袖线下齐聚南京,包括日本PMDA、印尼FDA、沙特SFDA、EMA等国际权威代表,共同探讨亚太与欧美监管协同策略。
“启明星奖” 作为 CGCS 2025 的核心亮点之一,由第六届国际细胞与基因治疗中国峰会暨展览会设立。该奖项聚焦 CGT、mRNA、小核酸、干细胞、外泌体、类器官、肿瘤新抗原等前沿赛道,覆盖早期研发、临床转化、生产工艺优化及商业化探索全链条。表彰先进疗法领域参与者的创新贡献,彰显中国CGT产业链的成熟度与国际竞争力。

近岸蛋白作为CGT产业链优质的上游原料和试剂供应商,深耕重组蛋白行业十余年,专注于蛋白技术与应用解决方案,为CGT客户提供GMP级别关键生产原料,助力客户成功IND。
在基因与细胞治疗中,近岸蛋白可提供全流程细胞因子供应服务,RUO级和GMP级产品确保客户无缝临床转化;在T细胞激活扩增上, 4.5μm的GMP级CD3/CD28 beads(Cat. No.:GMP-B016)选用人源化抗体,极大降低免疫原性风险;GMP级mRNA体外转录及修饰用酶、Cas9/AaCas12bMax/enCas12hf/enCas12Ultra蛋白,满足不同应用场景的基因编辑需求。全能核酸酶(BenzoNuclease)可高效降解任何形式的DNA及RNA,并已完成FDA DMF备案,可以满足药物申报的规范。
⭐规范的GMP生产环境和管理体系
按照药品生产GMP质量管理规范建立洁净生产车间,实行GMP质量管理体系保障物料及过程的可控性与可追溯性,制剂车间按照B级无菌制剂要求灌装,制剂采用药用辅料。
⭐符合多国药典规范
-
《药品生产质量管理规范(2010年修订)》
-
《GMP附录-细胞治疗产品》国家药品监督管理局
-
《中国药典》2020年版国家药典委
-
USP Chapter<92>和<1043>
-
Ph. Eur. General Chapter 5.2.12
⭐严格质量控制
-
采用无动物源性材料生产和药用辅料制剂
-
生产工艺具备完善的病毒灭活去除步骤
-
生产用细胞株按照中国药典要求进行全面检定,无病毒和外源因子污染
-
无菌、无氨苄青霉素、无支原体
-
药用西林瓶包装
⭐FDA DMF申报
已有17个GMP级产品获得美国FDA DMF申报,其中mRNA疫苗药物原料11个,生物药原料6个
⭐辅助药物申报文件
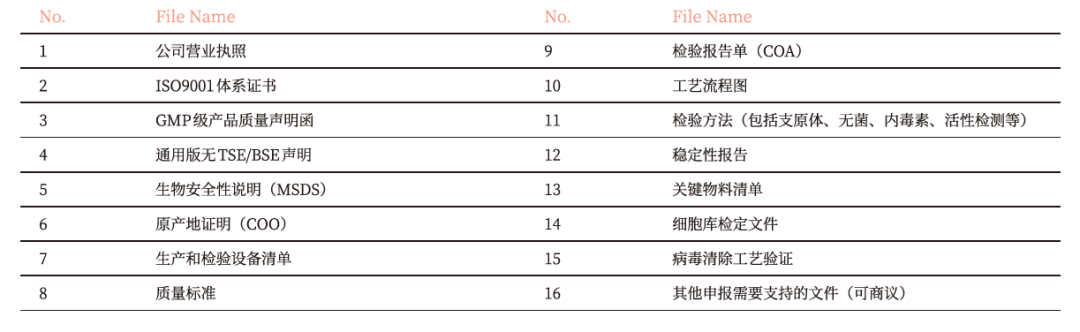
我们始终致力于为生物医药行业提供创新性蛋白质工具,同时积极联动产业链上下游企业,构建以实际应用需求为导向的技术创新生态体系。未来,我们将持续推出更多高品质原料,推动基因与细胞治疗产品的开发与商业化,为全球医疗健康事业的发展贡献力量。
